商机详情 -
山东值得信赖临床前动物实验研究
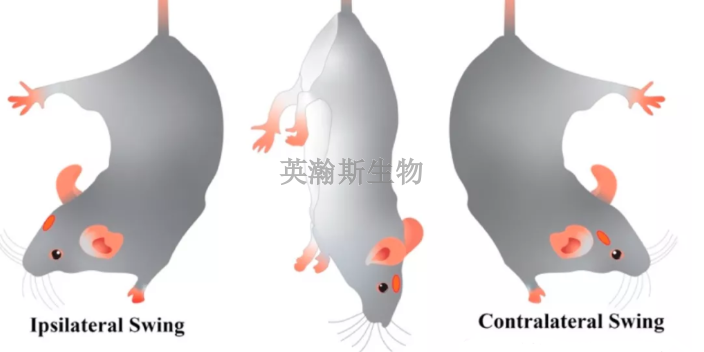
建议在临床前动物实验设计中设置一个对照组,或解释为什么不设置对照组。此外,应使用足够数量的动物来支持医疗器械安全性和性能的验证结果。动物数量的确定比较好在台架测试和器械的迭代研究完成之后。研究中动物的数量应基于合理的科学依据,并考虑到模型的难度,以及是否可在一只动物中合理研究一种或多种受试物和对照品。根据经验,较高级物种(例如,绵羊、山羊、非人灵长类动物)的典型动物实验研究通常每组/时间点有3~9只动物。但是,在任何情况下,方案中都应提供所用动物数量的科学依据。中成药临床前动物实验机构;山东值得信赖临床前动物实验研究
在慢性(长周期)研究中,入组的动物(如反刍动物)通常被转移到更典型的农业饲养环境中,允许动物在开放牧场放牧和/或喂食干草作为其饮食的组成部分。临床前动物实验研究机构应确保牧场没有潜在的有毒植物、寄生虫卵和其他潜在污染物,并且牧场的条件(土壤、草地)符合动物的营养需求,包括矿物质。一些物种可能对土壤中有机矿物质不平衡很敏感(例如,羊对铜和钼不平衡敏感),这可能会不经意地导致中毒(铜对羊的毒性)。生长促进剂,如莫能菌素是另一种常见的无意的毒性来源,这是由于定量配制中的错误或给一个物种喂养另一个物种的配比造成的。必须定期检查饲料和水,以确保已知可能干扰研究的污染物不会超出方案规定的水平。动物实验研究机构应认识到这些潜在问题,并在编写标准操作规程时处理这些问题,这些程序涉及定期测试水和饲料中潜在的污染物、牧场土壤和植物的营养平衡、培训员工阅读配给标签及喂特定物种相应的配比等。吉林高质量临床前动物实验哪家好化学药临床前动物实验公司;
临床前动物实验到Ⅰ期临床试验——安全之路?——TGN1412Ⅰ期临床试验的惨痛教训的相关知识。2007年1月27日,来自英国伦敦帝国学院、伦敦国王学院和Babraham研究所的学者报告,人体的记忆T细胞可能是2006年3月造成抗CD28人源化单克隆抗体(TGN1412)Ⅰ期临床试验悲剧的原因。抗CD28人源化单克隆抗体——TGN1412Ⅰ期临床试验灾难性意外是2006年医药行业的热点新闻。对此,英国成立的单独**小组(ESG)曾召开过10多次会议,并于2006年12月7日发布了比较终研究报告。英国药物和保健品管理局(MHRA)也将于2007年2月6日召开研讨会以探讨从TGN1412事件中吸取的教训。对这一事件的回顾与分析无疑有助于人们更深入的思考药物试验面临的一些问题。
临床前动物实验,科学家可以了解从神经元的真实生物物理模型,它们的动态交互关系以及神经网络的学习,到脑的组织和神经类型计算的量化理论等,并从计算角度理解脑,研究非程序的、适应性的、大脑风格的信息处理的本质和能力,探索新型的信息处理机理和途径。也就是说,借助这种方法,未来科学家可以对大脑进行结构和功能的模拟。计算神经科学中的模型并不是凭空创造的,它们依然是基于实验,从中得到数据才可以构建的。而比较终测试模型是否成立,依然需要回归到实验中去检验。因此,临床前动物实验和人体试验不可替代。中成药临床前动物实验多少钱?
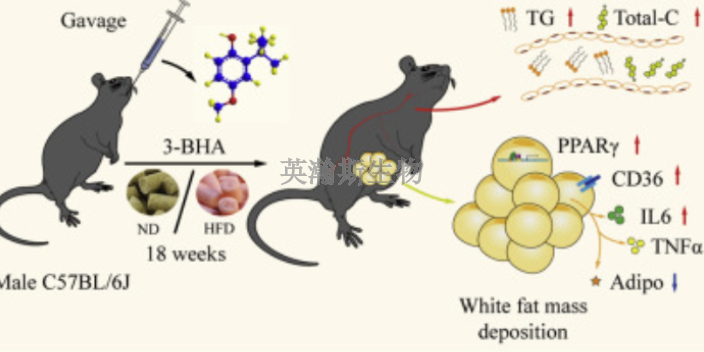
临床前动物实验安全性与有效性的关系:医疗器械临床前动物实验的主要目的是研究其安全性;生物相容性是医疗器械安全性的特征之一(如血液相容性和细胞毒性);有效性不是临床前评价的主要方向,而是它包含一定程度的有效性内容;建立适当的模型可以提高有效性研究的水平,可以作为临床前评价的重要内容,即试验装置的实际使用与预期使用的符合性。但这类研究成果不能作为医疗器械有效性评价的客观依据,只能作为能否转移到人体进行临床研究的辅助参考。对有效性的客观研究是不现实的,有时只是厂家一厢情愿地在动物实验中验证医疗器械的有效性。但也有一些例外,如结构性心脏病器械、血管疾病器械、止血材料等,都可以得到一定程度的验证。无论实验模型如何设计,都与器械预期使用的人体对象存在较大差异;很难设计和完成完全符合或接近预期人体对象的动物模型;医疗器械的临床研究是其有效性验证的关键阶段,也是其安全性的另一个验证(确认)阶段。生物药临床前动物实验价格;江西专业临床前动物实验评价
医疗器械临床试验前动物试验研究要点有哪些?山东值得信赖临床前动物实验研究
临床前动物实验的计划和实验方案制定:首先,临床前动物实验研究必须经过周密计划。为此,实验计划需要有一定资质的机构或者个人提出,由有适当资质和经验的指定的专题负责人进行指导。专题负责人宜在实验场所办公,便于指导和监督实验技术的实施。专题负责人负责研究结果的解释、分析、形成文件和报告。实验方案应包括《药物非临床研究质量管理规范》第八章第二十九条中所要求的适用于一般GLP方案的十五项要素,并宜包含如特殊环境下的研究规范(操作指南)。任何**终已通过的实验方案的改变和修改以及修改原因都必须经由专题负责人签字并签署日期。实验方案和任何修改必须提供给质量保证部门检查。研究开始前需要先通过动物伦理委员会对已确定的实验方案进行审批。山东值得信赖临床前动物实验研究