商机详情 -
Desmin免疫组化IHC
细胞免疫荧光实验常见问题:1、信号弱或者无信号:细胞或组织样本保存时间过长;2)抗体浓度不合适,参照抗体说明书的稀释浓度,再根据样本表达量进行摸索;3)一抗孵育时间不合适,建议 4 ℃ 过夜孵育。2、高背景:封闭不充分;抗体浓度过高;抗体孵育时间过长或温度过高;清洗不充分;样本变干,染色过程确保样品始终浸没于液体环境中.3、非特异性染色较多:固定液残留,这里需要缩短固定时间并且在封闭液中加甘氨酸,并且抗原修复也可以帮助解决非特异性染色;二抗残留,二抗需要用带有吐温 20 的 PBS 溶解,只要荧光显微镜的强度还可以增大,那么就可以增加吐温洗脱掉非特异性染色。免疫荧光技术可以用于研究免疫系统的功能和异常。Desmin免疫组化IHC
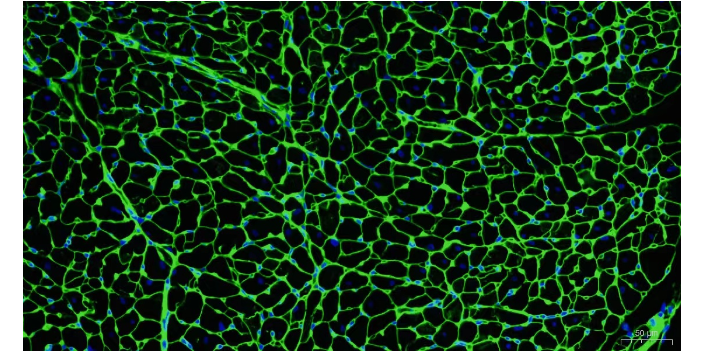
细胞的固定及免疫荧光:1)吸除培养基,一般先加入PBS浸洗细胞 3 次,每次 5 min。2)向孔内加入4%多聚甲醛1ml,进行细胞固定,室温固定20分钟。3)吸去多聚甲醛,使用PBS浸洗 3 次,每次 5 min。4)向孔内加入0.5%Triton X-100(PBS配制)室温通透20min,目的是使细胞通透。5) 除去Triton X-100,使用PBS浸洗 3 次,每次 5 min。6)用10%的与二抗同源的山羊血清(PBS配制)或者5%BSA封闭2小时(选择的封闭液与后面操作过程中抗体稀释液一致)。封闭后不需要用PBS清洗。7)吸去封闭液,向每孔滴加足够量适宜浓度的一抗(一次使用抗体可以根据抗体说明书推荐浓度,后续实验可以摸索抗体的适宜浓度),4℃湿盒内孵育过夜。ERK免疫荧光荧光抗体法和荧光抗原法都属于免疫荧光技术的范畴。
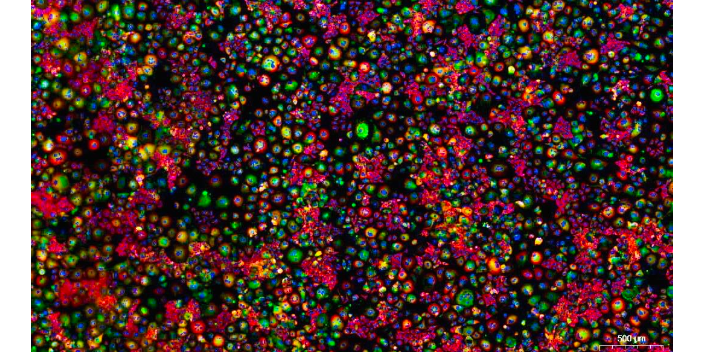
细胞免疫荧光实验注意事项:非特异性染色:是否灭活内源性过氧化物酶;孵育过程中干片;抗原热修复过度。染色过深:一抗浓度过高;染色试浓度过高或孵育时间过长;染色剂浓度过高或孵育时间过长。通常实验室先固定细胞再进行通透,但若检测抗原是水不溶性蛋白,可先通透再固定,这样可以通过通透去除一些水溶性蛋白,进而可降低免疫荧光背景和非特异性信号;建议设阴性对照组,消除由于抗体非特异性结合而产生的背景染色;选择醛类固定液时,保持其新鲜度,较好现配现用,使用不新鲜的醛类固定液自发荧光背景会升高。
免疫荧光固定(防止离体组织自溶抗原扩散),固定液包括:有机溶剂(甲醇、乙醇等);交联剂(4%PFA、10%中性福尔马林),固定液的选择取决于被研究抗原的性质及所用抗体的特性,不过,目前甲醛用的还是较多的,但针对磷酸化的抗体,不适合用甲醛,会导致磷酸蛋白从膜表面转移到胞浆中,故应选择冰冷的无水甲醇或无水乙醇,同时应注意甲醛会挥发,在4-8°C不宜储存太久。固定时间:取决于组合块的大小和类型,对于大多数组织,18-24h较为理想,细胞固定时间较短,一般2%的甲醛室温固定20min即可。以细胞样品为例:用4%的多聚甲醛固定爬片15min,PBS浸洗玻片3次,每次3min。免疫荧光技术在免疫学研究中发挥重要作用,帮助揭示细胞和分子的功能和相互关系。
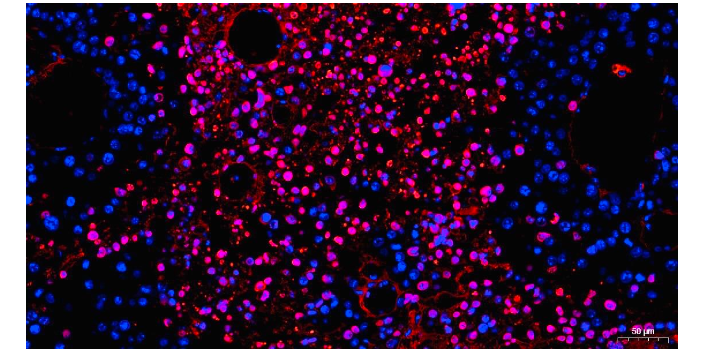
免疫荧光的原理和类型:免疫荧光利用荧光分子或荧光团在一定波长(分子的吸收光谱)下吸收光子的特性,经过短暂的间隔(发射光谱)后以较高的波长发射光子,并伴随能量损失。发射的荧光可通过显微镜观察到。荧光团可以通过可见光或紫外光激发。具有高光稳定性和荧光量子产率的荧光染料可在市场上购买,其激发较大值跨越从400到>700nm的波长范围。它们不会损伤活细胞,可安全用于生物制剂。在进行免疫荧光检测时,首先对细胞或组织进行固定和透化处理。进行免疫染色时,荧光团与目标抗原的抗体结合,然后使用成像显微镜观察荧光信号。根据使用的抗体和所需的信号扩增,免疫荧光可分为直接和间接两种类型。免疫荧光技术可以用于研究肉瘤的发生和发展过程。ERK免疫荧光
免疫荧光技术可以用于研究疾病的发生机制和医治效果评估。Desmin免疫组化IHC
免疫荧光注意事项:对照实验的设置:1、内源性组织背景对照:某些细胞和组织可能有固有的生物学性质,会产生背景荧光,对结果产生影响,例如色素脂褐质。因此在孵育一抗前,应对样品进行观察,确保抗原本身没有信号。2、阳性对照:用确认含有待测抗原的组织或细胞,与待测标本进行统一处理,结果应为阳性,可证明待测抗原有一定活性并且实验过程中用的试剂及方法均可靠。3、阴性对照:与阳性对照相反,用明确不含有待测抗原的细胞或组织切片染色,结果若为阴性,可排除染色过程中由于非特异性染色造成的假阳性结果。Desmin免疫组化IHC