商机详情 -
湖南染色体蛋白互作ChIP
Q:ChIP-Seq和ChIP-qPCR有何异同?A:染色质免疫共沉淀(ChIP)所获得的DNA产物,在ChIP-Seq中通过高通量测序的方法,在全基因组范围内寻找目的蛋白(转录因子、修饰组蛋白)的DNA结合位点片段信息;ChIP-qPCR需要预设待测的目的序列,针对目的序列设计引物,以验证该序列是否同实验蛋白结合互作。
Q:染色质片段大小在哪个范围比较合适?A:对于ChIP-seq,片段在200-500bp左右是合适范围;对于ChIP-qPCR,片段在200-800bp左右适宜。
Q:植物样本处理和动物组织/细胞有何区别?A:植物组织由于细胞壁、气腔等结构的存在,会给交联缓冲液的作用带来困难,因此相对于动物组织/细胞来说,往往需要在抽真空条件下进行交联,而该步奏是一个需要经验及优化的过程。
Q:ChIP-Seq中的测序DNA样本需要多少产量?A:通常是≥10ng。
Q:ChIP风险如果判断A:ChIP实验以标签来判断实验风险,重组标签的转录因子>内源转录因子>组蛋白;当以重组蛋白作为靶蛋白时,重组蛋白同内源蛋白可能存在结合活性、结合位点差异;以标签抗体进行ChIP时、染色质结合位点本身会被内源蛋白竞争,这些都会影响到ChIP过程的特异性捕获效率。 ChIP实验通常只能检测与特定抗体结合的蛋白-DNA复合物,可能无法检测到所有与目的基因结合的蛋白。湖南染色体蛋白互作ChIP

ChIP-seq与ChIP-qPCR在实验技术、分辨率和数据分析方面存在明显的不同之处。首先,ChIP-seq结合了高通量测序技术,能够在全基因组范围内检测蛋白质与DNA的结合位点。它通过测序仪对富集的DNA片段进行大规模并行测序,生成海量的数据,从而提供高分辨率的结合位点信息。相比之下,ChIP-qPCR则侧重于对特定基因或基因区域进行定量分析,它通过荧光定量PCR技术检测富集的DNA片段的数量,具有更高的灵敏度和特异性,但只能针对已知序列进行分析。其次,ChIP-seq在分辨率上优于ChIP-qPCR。由于ChIP-seq可以对全基因组进行测序,它能够检测到更多的结合位点,包括那些低丰度或远离转录起始位点的结合事件。而ChIP-qPCR则受限于所选择的基因或基因区域,可能无法全局反映蛋白质在基因组上的结合情况。在数据分析方面,ChIP-seq生成的数据需要进行复杂的生物信息学分析,包括序列比对、峰值调用、注释和富集分析等步骤。而ChIP-qPCR的数据分析相对简单,主要通过比较不同样品间的荧光信号强度来判断蛋白质的结合情况。贵州染色质蛋白互作检测ChIP作为ChIP实验的初学者,应该注意哪些问题。
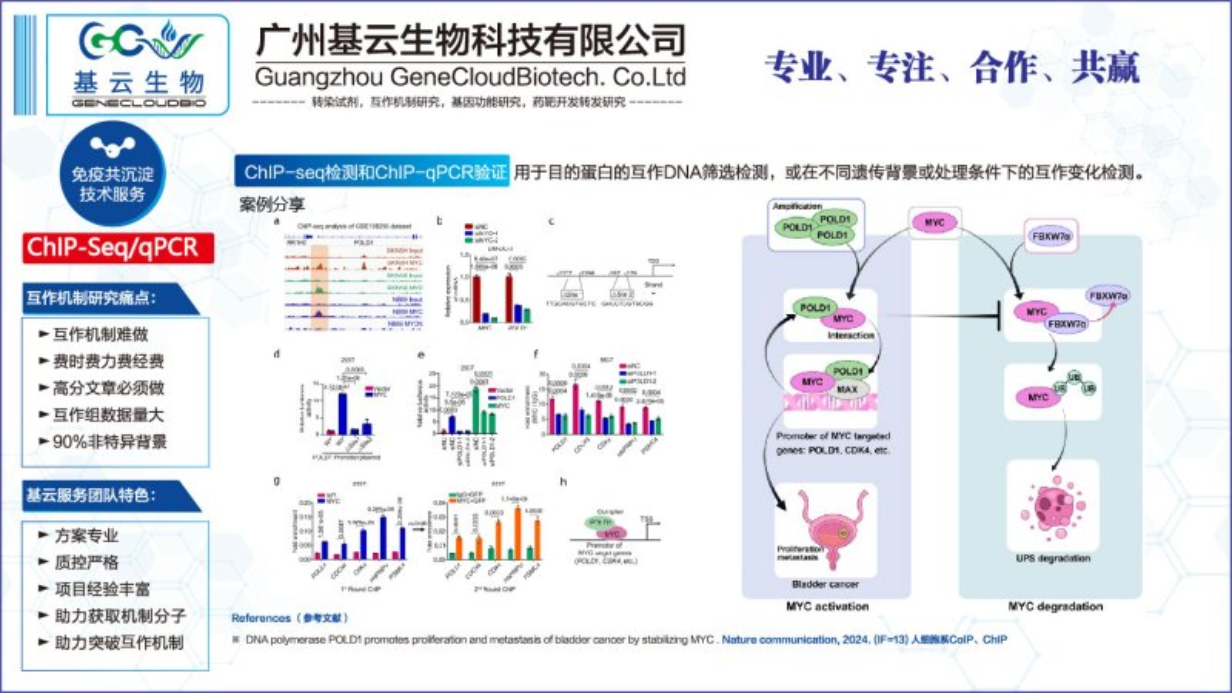
ChIP-qPCR实验流程主要包括以下步骤:交联与裂解:首先,将细胞或组织进行交联处理,以固定蛋白质与染色质的相互作用。常用的交联剂如甲醛。交联后,使用裂解缓冲液裂解细胞核,释放染色质的DNA。染色质片段化与免疫沉淀:接着,对染色质进行切割,生成适当大小的DNA片段,这些片段包含特定的蛋白质结合位点。然后,将特异性抗体加入样品中,与目标蛋白质结合形成免疫复合物。这些抗体是针对目标蛋白质的特异性抗体。洗涤与解交联:通过洗涤缓冲液去除非特异性结合物和杂质,保留具有特异性结合的免疫复合物。之后,通过加热或酶解等方法去除DNA与蛋白质之间的交联,释放DNA。DNA纯化与qPCR分析:使用DNA提取试剂盒等方法纯化免疫沉淀得到的DNA片段。随后,将提取的DNA片段进行qPCR反应,通过监测荧光信号变化,对目标基因进行定量分析。以上即为ChIP-qPCR实验的基本流程,实验结果可用于揭示蛋白质在基因组上的结合位点及转录调控机制。
ChIP-qPCR实验是一种结合染色质免疫沉淀(ChIP)与实时荧光定量PCR(qPCR)的技术,具有独特的实验意义和应用价值。首先,ChIP-qPCR实验可以验证特定转录因子或其他蛋白质与特定DNA序列的结合情况。这对于确认已知的蛋白质-DNA相互作用以及深入探究其结合机制和功能非常重要。通过这种方法,研究人员可以精确地定位蛋白质在基因组上的结合位点,并进一步分析这些结合事件对基因表达调控的影响。其次,ChIP-qPCR实验相对简单、快速且成本较低,适用于小规模的研究和初步筛选。它允许研究人员在有限的资源和时间内获得关于蛋白质-DNA相互作用的有价值的信息。此外,通过设计特异性引物,ChIP-qPCR可以实现对目标区域的精确定量,从而提供关于蛋白质结合程度和动态变化的定量数据。这些数据有助于揭示转录调控、染色质结构和功能以及细胞信号传导等方面的机制。因此,进行ChIP-qPCR实验对于理解基因表达调控、解析细胞内的复杂生物过程以及开发潜在的诊疗策略具有重要意义。如何快速入门ChIP实验。
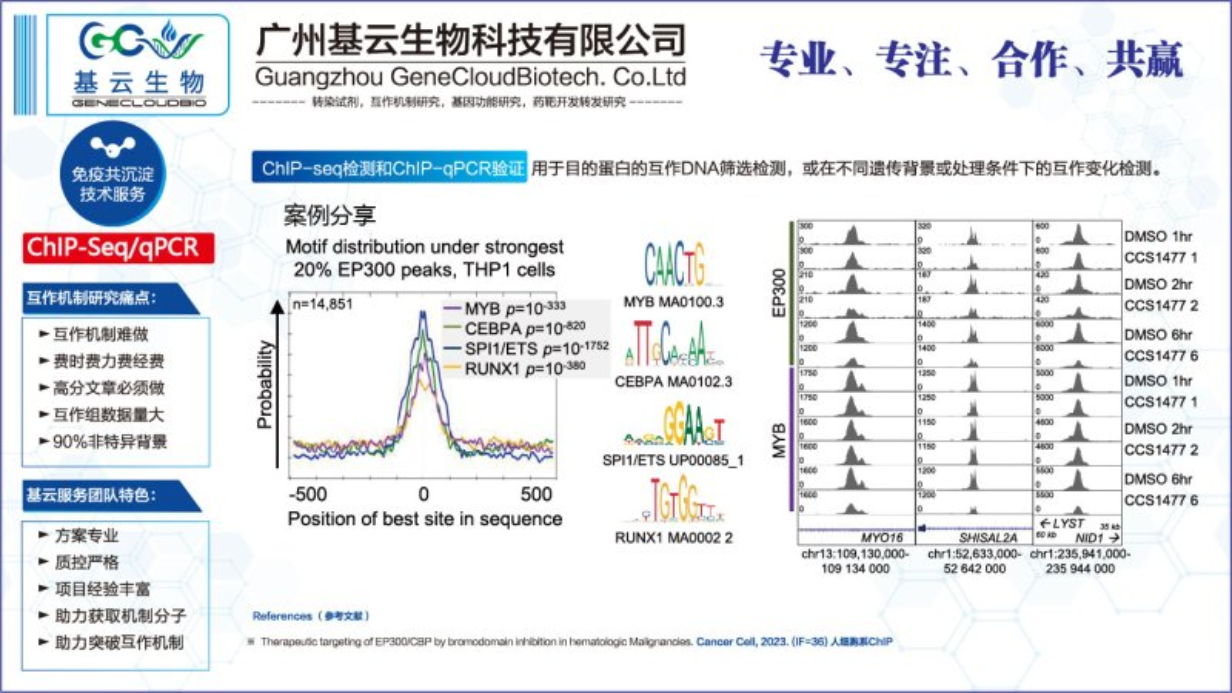
ChIP-qPCR和ChIP-seq实验在多个方面存在异同点。首先,在实验流程上,两者都包含染色质免疫沉淀这一关键步骤,用于富集与特定蛋白质结合的DNA片段。然而,在后续的检测方法上,它们有所不同。ChIP-qPCR采用实时荧光定量PCR技术对这些片段进行定量检测,适用于已知蛋白质与靶序列相互作用的研究。而ChIP-seq则结合了高通量测序技术,能够在全基因组范围内检测与特定蛋白质结合的DNA区域,适用于未知靶序列的探索。其次,在分辨率上,ChIP-seq具有更高的分辨率,能够提供完整、高分辨率的结合信息,绘制出转录因子等蛋白质在全基因组范围内的结合位点图谱。而ChIP-qPCR的分辨率相对较低,通常只能针对已知基因或基因区域进行分析。另外,在应用范围上,ChIP-seq在探索转录调控网络、表观遗传机制等领域具有更广泛的应用价值。而ChIP-qPCR则更适用于验证特定转录因子与基因启动子的结合等具体作用机制的研究。综上所述,ChIP-qPCR和ChIP-seq在实验流程、分辨率和应用范围上存在异同点,研究者应根据具体需求选择合适的技术方法。通过ChIP-qPCR分析转录因子结合位点的富集程度,为转录因子结合位点的功能研究提供实验依据。福建染色体蛋白互作ChIP
ChIP-qPCR实验虽然是一种有效的研究蛋白质与DNA相互作用的方法,但也存在一些缺点。湖南染色体蛋白互作ChIP
开展ChIP-qPCR实验时,应注意以下几个问题:实验设计:要有明确的实验目的,设计合理的对照组,比如设立IgG对照组以排除非特异性结合的影响。样品质量:保证使用的细胞或组织样品新鲜,且数量足够,避免因样品质量问题导致实验失败。抗体选择:选用高特异性和效价的抗体至关重要,要进行抗体的预实验验证其有效性。操作细节:严格按照ChIP的实验步骤进行操作,特别是在染色质片段化、免疫沉淀和洗涤过程中要控制条件,确保实验的重复性和准确性。避免污染:实验中要避免样品间的交叉污染和外界DNA的污染,使用无菌操作和无核酸酶的试剂。数据分析:在qPCR阶段要确保引物的特异性和扩增效率,对数据进行归一化处理,结合生物学背景和统计学方法进行合理解读。结果验证:建议通过多次重复实验进行结果的验证,增强实验结论的可靠性。安全防护:实验过程中要佩戴手套和防护眼镜,避免接触有毒有害试剂,确保实验室安全。通过注意这些问题,可以提高ChIP-qPCR实验的成功率和数据质量。湖南染色体蛋白互作ChIP