商机详情 -
嘉兴药理学膜片钳全细胞记录原理及步骤
膜片钳的数据如何处理:穿孔膜片(perforated patch)是为克服常规全细胞模式的胞质渗漏问题,有学者将与离子亲和的制霉菌素或二性霉素b经微电极灌流到含有类甾醇的细胞膜上,形成只允许一价离子通过的孔,用此法在膜片上做很多导电性孔道,借此对全细胞膜电流进行记录。由于此模式的胞质渗漏极为缓慢,局部串联阻抗较常规全细胞模式高,所以钳制速度很慢,也称为缓慢全细胞模式。它适合于小细胞的电压钳位,对于直径大于30μm的细胞很难实现钳位。不足之处是由于电极与细胞间交换快,细胞内环境很容易破坏,因此记录所用的电极液应与胞浆主要成分相同,如高k+,低na+和ca2+及一定的缓冲成分和能量代谢所需的物质。膜片钳技术用特制的玻璃微吸管吸附于细胞表面,使之形成10~100MΩ的高阻封接,被孤立的小膜片面积为微米数量级,因此封接范围内细胞膜光有少数离子通道。科研服务选品,膜片钳技术服务商推荐上海司鼎生物,专业度高。嘉兴药理学膜片钳全细胞记录原理及步骤

膜片钳技术:膜片钳技术是用玻璃微电极吸管把只含1-3个离子通道、面积为几个平方微米的细胞膜通过负压吸引封接起来,由于电极与细胞膜的高阻封接,在电极笼罩下的那片膜事实上与膜的其他部分从电学上隔离,因此,此片膜内开放所产生的电流流进玻璃吸管,用一个极为敏感的电流监视器(膜片钳放大器)测量此电流强度,就替代单一离子通道电流。膜片钳技术的建立,对生物学科学特别是神经科学是一资有重大意义的变革。这是一种以记录通过离子通道的离子电流来反映细胞膜单一的(或多个的离子通道分子活动的技术。些技术的出现自然将细胞水平和分子水平的生理学研究联系在一起,同时又将神经科学的不同分野必然地融汇在一起,改变了既往各个分野互不联系、互不渗透,阻碍人们很全认识能力的弊端。合肥细胞生物学膜片钳电生理技术原理及步骤在自动化系统辅助下,自动化膜片钳技术可实现稳定测量流程,降低人工操作。
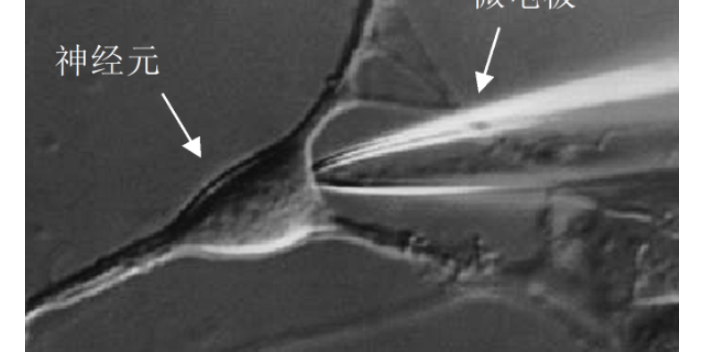
膜片钳技术之全细胞记录的实验流程:(1)仔细检查实验系统各仪器间的线路连接。(2)依次打开各仪器的电源开关和实验软件,检查各参数的初始设置。(3)将样品置于倒置显微镜的载物台上。(4)电极安装。(5)偏移电位的补偿和电极电阻的测定:在微操纵器控制下使微电极进入浴液,电流基线通常会立刻漂离零位,若此时处于VC模式,在维持电压为零时,通过调节偏移电位补偿,使电流基线等于零,此时可见基线上叠加有响应电流方波。(6)细胞封接。(7)电极电容补偿:若无特殊要求,一般将保持电位设为受试细胞静息电位平均值。
单细胞膜片钳技术是一种极具细致性的电生理记录方法,能够在单个细胞水平上捕捉离子通道的电流变化,为细胞功能的深入研究提供了坚实基础。该技术通过使用微玻管电极紧密接触细胞膜,形成高阻抗封接,隔离电极所接触的膜片区域,进而实现对该膜片或整个细胞内离子通道电流的监测。这种方法不仅能够揭示钠、钾、钙等离子通道的活动状态,还能够捕捉动作电位和突触后电流的细微变化,极大地丰富了对细胞生理状态的理解。选择可靠的单细胞膜片钳技术供应商对于科研团队来说尤为重要,因为这关系到实验数据的准确性和重复性。专业的供应商不仅提供高性能的膜片钳设备,还能提供完善的技术支持和定制化的解决方案,满足不同实验需求。上海司鼎生物科技有限公司便是这样一家专注于生命科学领域的企业,依托上海科研院所的技术积累,致力于为用户提供涵盖试剂、仪器和技术服务的综合支持。公司在单细胞膜片钳技术方面拥有丰富经验,能够协助科研人员优化实验流程,提升数据质量。在电生理学研究中,膜片钳技术可记录瞬时电流变化,为解析细胞信号调控机制提供数据。
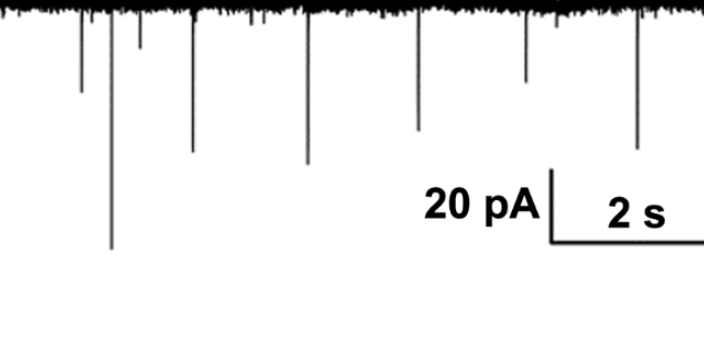
膜片钳电生理技术的样本种类:从较早的肌细胞、神经元和内分泌细胞发展到血细胞、肝细胞、耳蜗毛细胞、胃壁细胞、上皮细胞、内皮细胞、免疫细胞、精母细胞等多种细胞;从急性分散细胞和培养细胞发展到组织片乃至整体动物;从蜗牛、青蛙、蝾螈、爪蟾母细胞发展到鸡细胞、大鼠细胞、人细胞等;从动物细胞发展到细菌及植物细胞。此外,膜片钳技术还普遍地应用到平面双分子层(planarbilayer)、脂质体(liposome)等人工标本上。研究对象:从对离子通道(配体门控性离子通道、电压门控性离子通道、第二信使介导的离子通道、机械敏感性离子通道及缝隙连接通道等)的研究发展到对离子泵、交换体及可兴奋细胞的胞吞、胞吐机制的研究等。膜片钳电极已不单单是传统意义上的电信号记录电极,它还可作为其他研究方法的工具使用,如用于进行单细胞PCR技术时的细胞内容物抽吸。膜片钳技术(patch clamp)是当前研究细胞膜电流及离子通道的重要技术,被称为研究离子通道的“金标准”。合肥细胞生物学膜片钳电生理技术原理及步骤
记录细胞电活动,电信号膜片钳技术可准确捕捉信号,支撑功能分析。嘉兴药理学膜片钳全细胞记录原理及步骤
膜片钳实验实验,记录和分析数据准备工作就绪后即可进行实验操作,数据记录和分析。对电极持续施加一个1mV、10~50ms的阶跃脉冲刺激,电极入水后电阻约4~6MΩ,此时在计算机屏幕显示框中可看到测试脉冲产生的电流波形。开始时增益不宜设得太高,一般可在1~5mV/pA,以免放大器饱和。由于细胞外液与电极内液之间离子成分的差异造成了液结电位,故一般电极刚入水时测试波形基线并不在零线上,须首先将保持电压设置为0mV,并调节“电极失调控制“使电极直流电流接近于零。用微操纵器使电极靠近细胞,当电极尖锐端与细胞膜接触时封接电阻指示Rm会有所上升,将电极稍向下压,Rm指示会进一步上升。通过细塑料管向电极内稍加负压,细胞膜特性良好时,Rm一般会在1min内快速上升,直至形成GΩ级的高阻抗封接。一般当Rm达到100MΩ左右时,电极尖锐端施加轻微负电压(-30~-10mV)有助于GΩ封接的形成。此时的现象是电流波形再次变得平坦,使电极超极化由-40到-90mV,有助于加速形成封接。为证实GΩ封接的形成,可以增加放大器的增益,从而可以观察到除脉冲电压的首尾两端出现电容性脉冲尖锐端电流之外,电流波形仍呈平坦状。嘉兴药理学膜片钳全细胞记录原理及步骤