商机详情 -
辽宁小鼠实验动物模型推荐
实验动物模型,癫痫动物模型。癫痫是一种常见多发的慢性脑部疾病,以脑部神经元过度放电所致的突然出现反复和短暂的中枢的神经系统功能失常为特征。形成癫痫的原因多种多样,病理表现也各不相同。脑电图上的痫性发放和临床发作是癫痫的两个主要特征。痫性发放是局部神经元异常同步化活动在脑电图上的表现。作为大脑神经元活动的一种客观反映,目前通过脑电图检查发现痫样放电,仍是癫痫病诊断和癫痫灶定位的主要客观依据。 由于受条件的限制,人体癫痫脑电数据的样本收集比较困难,而且数据易受外界环境和患者运动的干扰,一些实验在道义和方法上也受到种种制约。如果能够先在实验室建立癫痫动物模型,通过对它进行实验并采集到大量样本,以验证现有算法的正确性,再进一步转向人体数据,就能克服这些不足,缩减科研工作的周期。 鉴于大鼠是医学研究中常用的一种实验动物,并且国内外已有几种可供选择的慢性癫痫模型,因此我们选择成年Wistar大鼠为实验对象,完成慢性颞叶癫痫模型的制备和数据的采集。英瀚斯生物,专业技术团队,熟练掌握各类实验动物模型构建。辽宁小鼠实验动物模型推荐
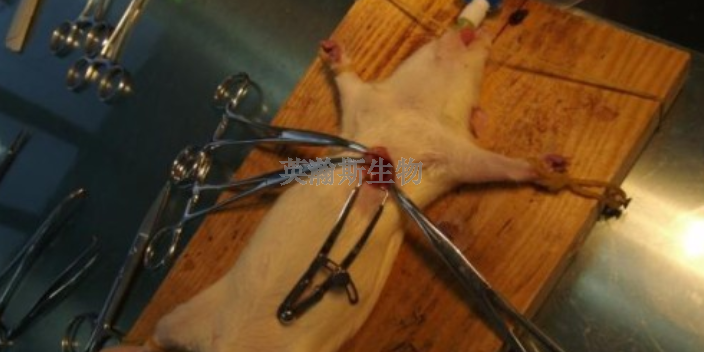
精神分裂症实验动物模型,英瀚斯生物小编为您介绍。旷场行为测试主要用于衡量动物的自发活动性和探索新异事物的行为,二者分别用动物在旷场测试中的水平运动距离和直立次数来衡量。有研究表明,慢性MK-801给药(NMDA受体拮抗剂)能诱导大鼠自发活动性的改变,自发活动距离的增加或减少与给药剂量及测试时间有关。在社会隔离建立的拟精神分裂症动物模型中,隔离组大鼠表现出旷场自发活动性的明显的增加。旷场自发活动性的增加与精神分裂症的阳性症状密切相关。辽宁提供实验动物模型检测哪家公司实验动物模型成功率比较高?
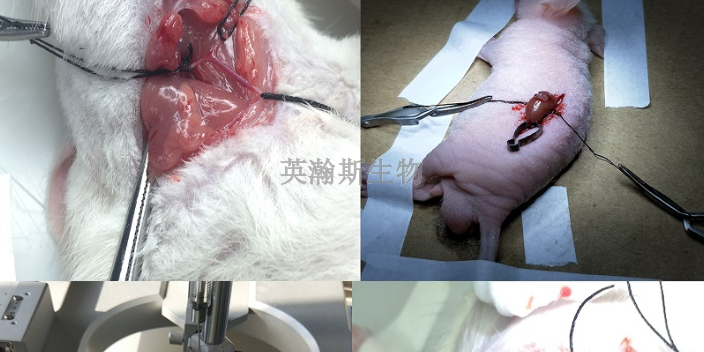
二型糖尿病实验动物模型:胰岛素抵抗和胰岛β细胞的功能缺陷胰岛素分泌异常
诱导方法一:小剂量STZ加高脂饲料诱导糖尿病模型。高脂饲料喂养4周后,腹腔注射STZ(30mg/kg),1周后选空腹血糖大于11.1mmol/L。
英瀚斯专业承接实验动物模型,欢迎实地考察实验室,来电咨询。
诱导方法二:转基因老鼠db/db小鼠:糖尿病小鼠(C57BL/KsJdb/dbmouse)也为Jackson实验室于1966年在C57BLKS/J(BKS)近交系中发现的自发性突变小鼠,该小鼠高糖、多尿及高尿糖水平的表型与人类的糖尿病患者非常相似。在10~14天出现高胰岛素血症,3~4周明显肥胖,在10周时可达野生小鼠的2~3倍,但身长比野生型短5%,并有高胆固醇血症和高甘油三酯血症。4~8周出现高糖血症,且表现出多食、消渴、多尿的典型糖尿病临床表现。
常见自发性实验动物模型1.免疫缺陷动物疾病模型1)B淋巴细胞缺陷疾病模型CBA/A小鼠,起源于CBA/H品系,特点是B淋巴细胞功能减退,为X-链隐性突变系,基因符号是Xid。临床表现为免疫球蛋白缺失,细胞免疫正常。2)T淋巴细胞缺陷疾病模型裸小鼠,主要特征为无毛、裸着的、无胸腺和细胞免疫功能丧失,由于第十一对染色体上等位基因突变引起。该鼠免疫能力低,易传染,生长不良,繁殖力低。这种动物能接受同种或异种组织移植,包括人cancer异种移植,可作为cancer免疫研究。国内常用裸小鼠品系为BALB/Cnu/nu,Swissnu/nu和NCnu/nu等,维持费较高。现也有裸大鼠、裸豚鼠等。图片2.自发性糖尿病动物模型KK糖尿病小鼠属先天遗传缺陷性小鼠。该鼠对胰岛素不敏感、对葡萄糖耐性小、糖尿病发病率高、老年鼠偶见肥胖。BBWistar大鼠是一种典型自发遗传Ⅰ型(胰岛素依赖性)糖尿病,发病率50-70%,临床表现为多饮、多食、gao血压、酮症、胰岛内β-细胞大量破坏等。NIH肥胖大鼠(SHR/N-cp)是新培育的一种用于肥胖和糖尿病研究的动物模型,表现出与人非胰岛素依赖性糖尿病相似的代谢改变。英瀚斯专业团队负责实验动物模型研究。

心血管疾病实验动物模型,英瀚斯生物小编为您介绍:1)动脉性粥样硬化动物模型常选用兔、猪、大鼠、鸡、鸽、猴和狗等。常用的方法有高胆固醇、高脂肪饲料法,免疫学法、儿茶酚胺药物注射法等。兔的优点为敏感性高,容易造成模型,时间短,缺点为它的脂质代谢与人类不同,兔表现为血源性泡沫细胞增多,解剖分布以胸动脉为主,小动脉常有病变。猪与人类相似,结合胸X-线照射,可引起冠状动脉痉挛。2)心肌缺血和心肌梗死电刺激法,雄兔麻醉后,用弱、强电交替刺激(0.8-1.6mA及4-6mA)右侧下丘脑背侧核,即可形成心肌缺血模型;药物法,给大鼠或兔注射异丙肾上腺素,狗静脉注射麦角新碱复制冠状动脉痉挛;冠状动脉阻断法,用大鼠或狗麻醉,在冠状动脉套上压迫环,复制心肌缺血和心梗模型。3)高血ya疾病动物模型可采用肾包扎法及肾动脉缩窄法复制继发性高血ya,用噪声刺激复制神经性高血ya模型。英瀚斯位于东南大学国家大学科技园,可承接实验动物模型制作。辽宁小鼠实验动物模型推荐
大鼠实验动物模型都有哪些?辽宁小鼠实验动物模型推荐
研究衰老的物理损伤实验动物模型。动物脑血流量老年期较成年期减少20%以上,脑部慢性缺血、缺氧使脑的正常功能受损,出现认知功能障碍等AD病理性改变。由此理论在实验研究中通过长久结扎双侧颈总动脉血管(2VO)建立的缺血性痴呆动物模型,表现出认知功能障碍明显,淀粉样蛋白前体升高、神经元和脑细胞死亡、tau蛋白过度磷酸化、氧化应激反应和产生慢性炎症等AD病理特征。该动物模型病程较长,在行为学表现上如认知功能障碍与AD比较一致,病理上也高度相似,但引起AD的外因在该动物模型中不能体现出来,另外,2VO动物模型手术操作具有一定难度,模型复制后动物存活率低且时间短,不适合给药周期长的实验研究。另外,还有长久性结扎单侧颈总动脉、去胸腺衰老模型和γ射线致衰老模型、控制性皮质撞击模型、液压脑损伤模型等,由于这些模型在造模方法上复杂、难度高、造模后动物容易死亡、且结果不理想,只在个别特殊目的实验中有所应用。辽宁小鼠实验动物模型推荐