商机详情 -
河北大鼠子宫内膜异位症模型实验外包
子宫内膜异位症(endometriosis,EM)是一种因子依赖性的常见良性变化,多发于生育年龄妇女,其发病率为10%-159毛。迄今为止,关于EM的真正发病机制并未比较终阐明,且缺少有效的治疗方法。其中一个主要原因是这种疾病只发生于人类和灵长类动物。由于实际操作和伦理学方面的约束,严重限制了对该疾病的研究,因此需要一种可在实验动物体内复制该病的方法。1922年Jacobson初次建立了兔的EM模型,从而开创了EM研究的新局面。本文就EM模型建立、应用的现状及进展进行综述。利用子宫内膜异位症模型,我们可以研究疾病对女性心理健康的影响。河北大鼠子宫内膜异位症模型实验外包
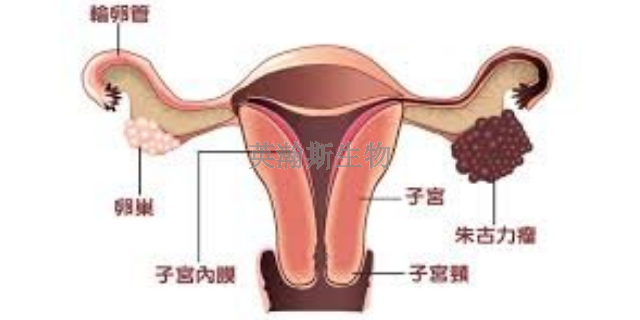
该子宫内膜异位症模型的建立,不仅有助于我们深入了解疾病的本质,更能帮助我们理解该疾病在不同人群中的差异表现。通过模拟不同人群的生理环境和遗传因素,模型能够呈现出子宫内膜异位症在不同个体间的差异性,如发病率、症状表现、疾病进展等方面的不同。这些差异性的揭示,使我们能够更普遍地认识子宫内膜异位症,为制定个性化的改善方案提供依据。同时,该模型还可以用于研究不同人群对改善方法的反应和预后情况,为提升改善效果和生活质量提供有力支持。因此,该模型在推动子宫内膜异位症的研究和改善方面发挥着重要作用。河北大鼠子宫内膜异位症模型实验外包通过子宫内膜异位症模型,我们可以研究疾病对女性生育能力的影响。
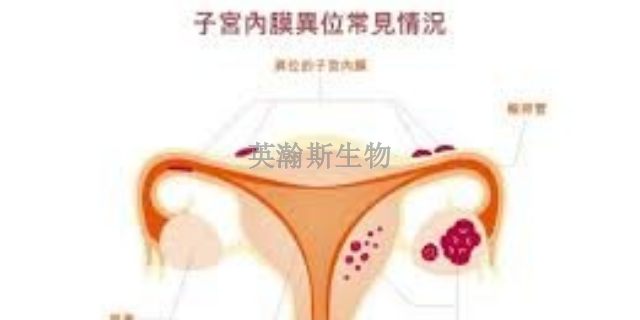
用于子宫内膜异位症模型的动物主要有灵长类动物和啮齿类动物,以及家兔、巴马香猪、鸡胚尿囊膜等。灵长类动物是***与人类相似、能自发形成EM的动物,因此是研究EM比较合适的动物模型。然而,由于实验动物缺乏、价格昂贵、饲养条件高、成模率低、实验周期长以及伦理学等多种原因限制了灵长类动物EM模型实验的研究。啮齿类动物由于价格便宜、易于获得、成模率高,被普遍采用。啮齿类动物包括大鼠和小鼠,其中免疫缺陷小鼠可进行异体移植[5,6,7],直接接受人体子宫内膜的移植,并且保留其原有特性,更接近人类疾病的病理变化,但由于其免疫功能缺陷,不能用来研究机体免疫方面的改变,且不能耐受多次手术和**检验。近年来,荧光EM小鼠模型的应用日益普遍,荧光动物模型是体内无创观察模型,其主观性小,病灶定位准确,能动态无损伤量化观察病灶生长情况,操作简单[8],但荧光表达时间有限,比较长只为4周,缺乏定量种植及观察标准。
子宫内膜异位症动物模型的建立与发展是为人类了解并改善EM提供基础,理想的动物模型应该尽可能与人类疾病相似,且规范化,能够准确地再现该疾病的特点,能可靠地反映疾病的发展变化,还应对临床有适应性和可控性,复制时经济易行。选择动物模型时应紧密围绕研究目的,权衡各种模型的利弊,充分发挥动物模型的优点,为临床研究提供指导。一些药物对EM模型有一定的作用,但需在人类进行进一步的证实。例如针对子宫内膜异位症模型的给药实验等 子宫内膜异位症模型为疾病的早期诊断提供了可能性。
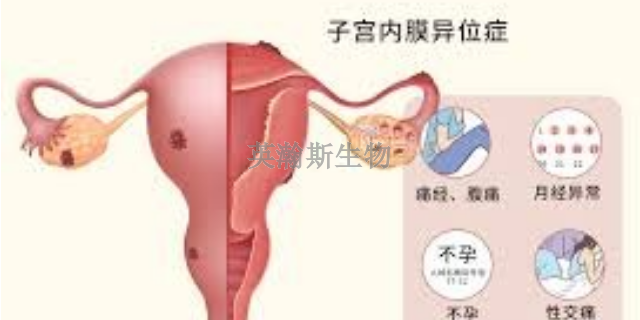
子宫内膜异位症模型的观察指标验证模型是否成功:大鼠建模28d后再次手术,腹腔麻醉后固定,腹部备皮,消毒铺巾,取原切口旁开腹,取出3个不同部位的移植物。记录移植物大体特点。用游标卡尺测量移植物的长度、高度与宽度,按公式计算体积:体积=0.52×长×宽×高[4]。用电子天平称取移植物质量。将取出的移植物和左侧子宫的在位内膜标本用10%多聚甲醛固定,常规石蜡包埋,H-E染色,显微镜下观察组织病理学变化来验证模型的成功率。子宫内膜异位症模型为研究疾病的免疫机制提供了重要的平台。安徽子宫内膜异位症模型有哪些
小鼠子宫内膜异位症模型怎么做?河北大鼠子宫内膜异位症模型实验外包
子宫内膜异位症模型的未来发展方向将聚焦于结合体外 $3\text{D}$ 细胞培养技术和体内基因编辑技术,以克服传统模型的局限性。子宫内膜类***模型(Endometrial Organoids)可以从患者的异位组织或正常组织中获取细胞,在体外重现腺体和间质的 $3\text{D}$ 结构,为高通量药物筛选和个性化药敏测试提供了新的平台。研究人员可以在体外环境中精确控制***和细胞因子的浓度,研究 $\text{EM}$ 细胞的增殖、迁移和侵袭能力。同时,利用 $\text{CRISPR-Cas9}$ 等基因编辑技术创建具有特定基因突变(如与 $\text{EM}$ 易感性相关的基因)的小鼠模型,可以更精确地模拟人类疾病的遗传易感性,并研究特定信号通路在疾病发生中的作用。将体外的类***模型与体内的基因编辑动物模型相结合,将是未来 $\text{EM}$ 研究的主流趋势,有望构建出更加完善、更具临床预测价值的复杂疾病模型系统。河北大鼠子宫内膜异位症模型实验外包